


三阴乳腺癌细胞免疫疗法治疗,三阴乳腺癌CAR-T细胞免疫疗法治疗
乳腺癌中的"顽敌"——三阴乳腺癌
乳腺癌是女性最常见的恶性肿瘤之一,全世界每年约有140万妇女发生乳腺癌,有50万妇女死于乳腺癌。而在乳腺癌家族中,有一位“癌中恶霸”——三阴乳腺癌,让患者痛不欲生,医生束手无策。其实乳腺癌并不是我们所认为的,只是单一的一种癌症。事实上,乳腺癌分为腔面A、腔面B、HER-2阳性和三阴性四种亚型,其中三阴乳腺癌属于最“毒”的一种。
三阴乳腺癌是指雌激素受体(ER)、孕激素受体(PR)和人表皮生长因子受体2(Her2)三个主要治疗靶点均为阴性的乳腺癌。在所有乳腺癌中,三阴乳腺癌占10%~17%,而且具有预后差、耐药性强、复发率高、治疗手段少等特点,成为乳腺界一大难题。
提到CAR-T疗法,有些人可能想到的就是抽取几管血,分离其中的免疫细胞,在体外进行扩增和改良,然后再回输给癌症患者体内。乍一听觉得CAR-T疗法很神奇,甚至有些天方夜谭。其实这一疗法并不简单,对于部分血液肿瘤患者来说,CAR-T疗法确实非常有效。
目前,随着CAR-T代数的更迭,CAR-T在增殖、细胞因子释放等方面有了明显改进,这一技术终于破冰,越来越多的临床试验开始尝试将CAR-T细胞疗法用于三阴乳腺癌。
CAR-T疗法打破僵局,三阴乳腺癌初迎曙光
2018年圣安东尼奥乳腺癌研讨会上,根据正在进行的I期研究的结果。CAR-T治疗晚期三阴乳腺癌(TNBC)获得了长期病情稳定,我们一起来看看具体研究情况。
西雅图华盛顿大学医学博士Jennifer Specht提供了7名表达ROR1的三阴性乳腺癌(TNBC)患者的数据,他们正在接受5个剂量水平的CAR-T细胞治疗。ROR1是一种孤儿酪氨酸激酶孤儿受体,在TNBC和非小细胞肺癌中表达。这些患者器官功能良好和表现状态尚可及可测量的疾病,免疫组化检测ROR1表达>20%。
ROR1的胚胎表达很高,但在成体细胞中的表达是有限的。乳腺癌中高水平的ROR1表达与预后不良有关,经常耐药。 这项研究还在招募患者,到目前为止,已经治疗了7名患者,现在CAR-T细胞的剂量水平已经调至3级,回输T细胞量高达3.3 x 10^6 个/ kg。这些患者先去接受过很多治疗,到目前为止,并没有发现明显的剂量限制性毒性。 只有1名患者发生了3级细胞因子释放综合征[CRS],但地塞米松和托珠单抗治疗后反应迅速。我们能够检测到大多数患者CAR-T细胞的扩增,但没有检测到特别高的水平。没有发现任何与ROR1表达相关的其他毒性,没有严重的病例神经毒性,严重的CRS或肿瘤溶解综合征。
所有接受治疗的患者(年龄范围27-67岁)至少有3线既往转移治疗的经历。3名患者接受多达9个前线治疗(1线代表一种方案,治疗无效换另一种方案,即2线,3线……),1名11个前线治疗。
最后的结果也令人惊喜,经CAR-T治疗后,患者的病情持续时间延长,一个达15周,另一个达19周,没有任何后续治疗方案的治疗效果超过CAR-T细胞。
另外,有一个患者第一次回输CAR-T后病情稳定,第二次回输后部分应答持续14周之久(对于晚期三阴乳腺癌,延长一周生存期就很不容易了!!)。(要想了解更多关于CAR-T国内外前沿临床研究信息请咨询无癌家园)
经典案例赏析:全球首次CAR-T疗法无进展生存乳腺癌末期!扩散全身的癌细胞完全消除
2018 年 6 月 4 日发表于《Nature Medicine》杂志上的一项临床研究中,美国国家癌症研究所使用免疫疗法(CAR-T),利用患者自身的免疫机制,将一晚期乳腺癌伴全身转移的女性病例成功无进展生存。
朱迪·伯金斯是一名来自美国佛罗里达州的工程师,当被选为此次新疗法的受试者时,她49岁,罹患乳腺癌,经历了数个疗程的化疗失败,癌细胞已从右乳扩散至肝脏及全身各处,预期寿命只有3年。
医生从朱迪·伯金斯女士体内注射约八百亿精心筛选的免疫细胞,同时应用派姆单抗(Pembrolizumab),一种阻断靶点为PD-1受体的细胞通路的抗体新药,它能够激活机体免疫系统攻击黑色素瘤细胞。
接受治疗42周之后,多项检验显示伯金斯女士体内已没有癌细胞。该患者至今仍然保持健康。这是史无前例的一次突破,免疫疗法在治疗乳腺癌上能够取得如此进展令人震惊。
另辟蹊径,MUC1 CAR-T疗法显著抑制乳腺癌的生长
1、MUC28z CAR-T细胞疗法:三阴性乳腺癌
2019年5月24日,北卡罗来纳大学夏洛特分校研究人员在《Immunol》杂志上公布了在异种移植模型中,单剂量的MUC28z CAR-T细胞可显著抑制三阴性乳腺癌(TNBC)肿瘤的生长的临床研究。
超过90%的乳腺癌患者中,MUC1过表达且糖基化异常。所以与肿瘤相关的MUC1是侵袭性表型的标志物,并用作靶向免疫治疗的肿瘤新抗原。因此,研究人员采用TAB004(一种高度特异性地针对tMUC1的单克隆抗体)工程MUC28z(一种嵌合抗原受体)融合分子来生成CAR T细胞,并对这些T细胞进行了表型和功能分析,结果发现MUC28z CAR-T细胞不管是在小鼠体内还是体外均能够有效抑制TNBC肿瘤的生长,具有针对tMUC1阳性TNBC肿瘤的高治疗潜力,并且对正常乳腺上皮细胞的损害较小。
由于tMUC1在包括胰腺导管腺癌和多种乳腺癌亚型在内的大多数上皮来源的实体瘤中广泛表达,因此MUC28z CAR-T细胞可能会在靶向实体瘤方面广泛应用。
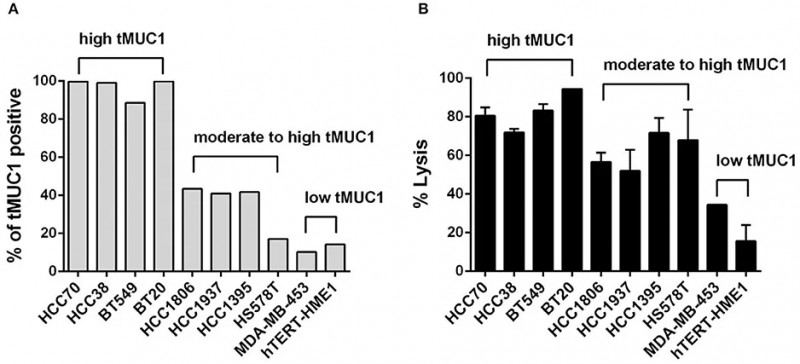
图示MUC28z CAR T细胞以抗原依赖性方式在体外裂解TNBC肿瘤细胞
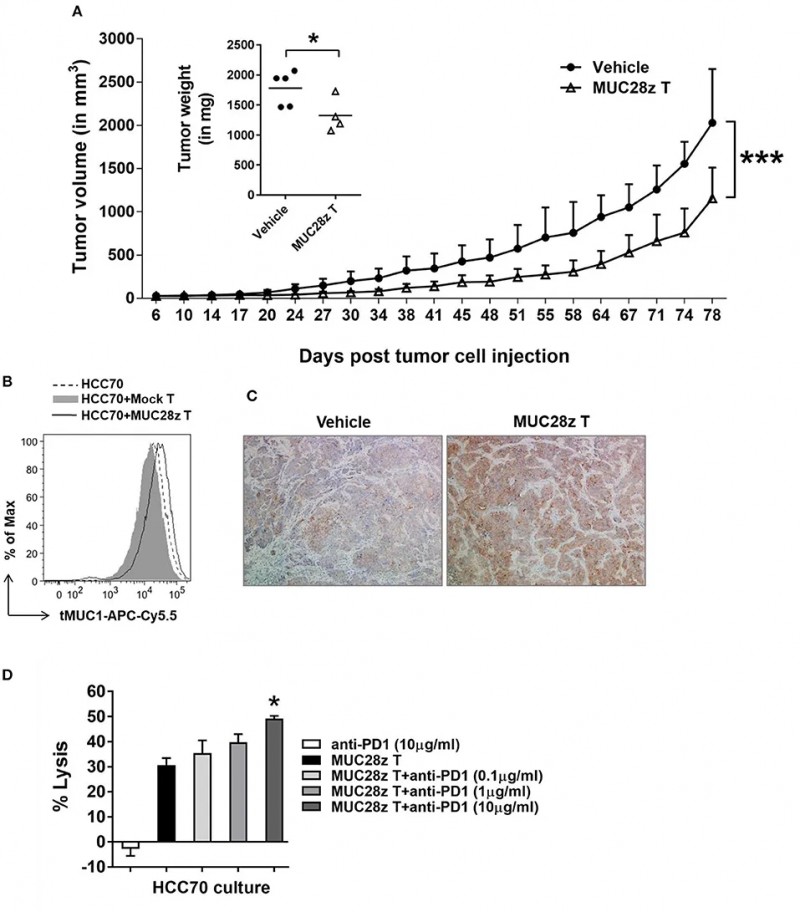
图示MUC28z CAR T细胞具有体内缩小HCC70肿瘤的长期疗效
2、huMNC2-CAR44 T细胞疗法:转移性乳腺癌
2019年6月24日,Minerva Biotechnologies(一家生物制药公司,专注于开发癌症免疫疗法)宣布,美国FDA已批准huMNC2-CAR44 T细胞疗法的研究性新药申请(IND),将对huMNC2-CAR44用于转移性乳腺癌进行临床试验,其靶向乳腺癌中MUC1(存在于超过75%的实体瘤癌细胞中)裂解产物MUC1 *生长因子受体。
之前针对MUC1的癌症疗法的尝试都失败了,因为它们是以全长的MUC1中在肿瘤细胞上被切割然后脱落并从癌细胞表面释放的那一部分为靶点。Minerva对仍然存在于癌细胞的部分MUC1(MUC1 *)、其活化配体和下一代CAR-T技术方面展开广泛专利布局。
MUC1靶点的发现推动了CAR-T细胞疗法在实体瘤中应用的进展,国内博生吉、荣泽生物等专注于细胞、免疫疗法的公司在针对MUC1靶点的CAR-T细胞疗法中也取得了不错的成果。
Minerva打算在2019年底之前开始乳腺癌的临床试验。“我们很高兴我们很快就能开始转移性乳腺癌的人体临床试验,”Minerva首席执行官Cynthia Bamdad博士说。“超过95%的乳腺癌呈MUC1 *呈阳性,这种癌症免疫疗法有可能为数千名与这种可怕疾病作斗争的患者带来希望。”
国内CAR-T细胞治疗实体瘤临床研究进行中
除了上述关于CAR-T的突破性临床研究外,目前国内正在积极开展实体瘤的CAR-T临床研究。
小编有话说
近年来,科学家们已经做出了相当大的努力来开发新的方法攻克实体瘤的障碍,并采用优化策略用于针对这些特定适应症的CAR-T疗法。我们期待着,越来越多的临床前/临床试验数据能够拼凑出一幅完整的拼图,充分展示CAR-T细胞疗法治疗实体瘤的真正实力。
参考文献
1.https://www.researchgate.net/publication/325552000_Immune_recognition_of_somatic_mutations_leading_to_complete_durable_regression_in_metastatic_breast_cancer
2.https://www.onclive.com/conference-coverage/sabcs-2018/initial-results-of-car-tcell-therapy-study-show-tolerability-in-vivo-expansion-in-tnbc
2. 备注【癌种】申请方舟援助计划


患者咨询电话:400-666-7998

全球肿瘤医生网提醒患者:国内细胞免疫治疗技术,包括cart细胞,树突细胞疫苗,NK细胞
TILs细胞,TCR t细胞治疗癌症疫苗等技术均处于临床试验阶段,未获准在医院正式使用。国内患者可以参加正规临床试验,在医生的监管下使用,全球肿瘤医生网不推荐患者贸然尝试任何医疗机构和研发机构的收费治疗。
本网站新闻资讯、文章、研究数据、治疗案例均来自于国内外医学论文,所涉及到的新药、新技术有可能还处于临床研究阶段,患者不能作为治疗疾病的依据。癌症治疗目前尚无治愈手段,患者需要在医生的指导下,在医院接受正规治疗或参加新药新技术临床试验。

-

-
肿瘤电场疗法——被FDA批准治疗复发性胶质母细胞瘤等
目前电场疗法已被FDA批准用于治疗复发性胶质母细胞瘤、新诊断的胶质母细胞瘤以及恶性胸膜间皮瘤,并且在目前在六大实体肿瘤包括非小细胞肺癌 详细»
-

-
临床试验中心——每一个新药都是一份希望
提供癌症临床试验招募信息、抗肿瘤新药受试者招募信息。 详细»
-
-
速递|三阴乳腺癌新辅助治疗,派姆单抗获批用于三阴乳腺癌新辅助疗法和三阴乳腺癌辅助疗法
2021年7月27日,FDA再次批准了派姆单抗的三阴性乳腺癌新适应症,分别用于辅助及新辅助治疗。 详细»
-
-
中国国产原研第二代免疫双抗药,双特异性抗体药物KN046联合白蛋白紫杉醇治疗转移性三阴性乳腺癌患者无进展生存7.3个月
本届AACR年会上,我国自主研发的免疫“双抗”KN046联合白蛋白紫杉醇治疗转移性三阴性乳腺癌患者的疗效公开,令人惊艳。 详细»
-

-
乳腺癌免疫疗法,四大乳腺癌免疫治疗方案能否扛起2021年乳腺癌治疗的大旗
免疫疗法被誉为癌症治疗的“第三次革命”,为包括乳腺癌在内的各癌症的治疗带来了革命性的变革。 详细»
-
-
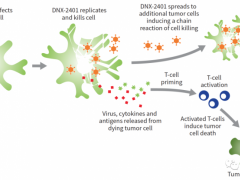
乳腺癌最新疗法,溶瘤病毒疗法治疗成为治疗乳腺癌的新武器
免疫疗法被誉为癌症治疗的“第三次革命”,通过诱导、增强或抑制免疫反应治疗疾病。 详细»
-
-
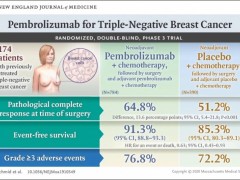
三阴乳腺癌新药,三阴乳腺癌免疫治疗(pd1)药物K药获FDA首批
2020年11月13日,美国食品药品监督管理局(FDA)批准了加速批准了默沙东(MSD)重磅PD-1抑制剂K药与化疗联用。 详细»
-

-
三阴乳腺癌免疫治疗成功案例
它被称为阿特珠单抗(也称为MPDL3280A,由Roche / Genentech制造),属于检查点抑制剂的免疫疗法。 详细»
-

-
三阴乳腺癌免疫治疗,三阴乳腺癌新药,三阴乳腺癌免疫疗法(PD-1/PD-L1)新药力挽狂澜
无进展生存期延长一半、客观缓解率53%,免疫疗法是怎样改变三阴性乳腺癌患者的治疗标准的? 详细»
-

-
2020年EMSO大会免疫联合化疗,三阴乳腺癌免疫治疗联合化疗改善生存率效果明显
在EMSO2020大会上,美国麻省总医院医学博士Aditya Bardia 讨论了先前接受sacituzumab govitecan治疗的转移性三阴性乳腺癌3期ASCENT随机试验的结果。 详细»




























 首页
首页 咨询
咨询 方舟新药
方舟新药 营养商城
营养商城